PROSPECT: INFORMAŢII PENTRU UTILIZATOR
MEPACT 4 mg pulbere pentru suspensie perfuzabilă
Mifamurtidă
Citiţi cu atenţie şi în întregime acest prospect înainte de a începe să utilizaţi acest medicament.
-Păstraţi acest prospect. S-ar putea să fie necesar să-l recitiţi.
-Dacă aveţi orice întrebări suplimentare, adresaţi-vă medicului dumneavoastră.
-Dacă vreuna dintre reacţiile adverse devine gravă sau dacă observaţi orice reacţie adversă nemenţionată în acest prospect, vă rugăm să-i spuneţi medicului dumneavoastră.
În acest prospect găsiţi:
1 Ce este MEPACT şi pentru ce se utilizează
2 Înainte de utilizarea MEPACT
3 Cum se utilizează MEPACT
4 Reacţii adverse posibile
5 Cum se păstrează MEPACT
6 Informaţii suplimentare
1. CE ESTE MEPACT ŞI PENTRU CE SE UTILIZEAZĂ
MEPACT conţine substanţa activă, mifamurtidă, similară unei componente a peretelui celular al unor anumite bacterii. Aceasta stimulează sistemul dumneavoastră imunitar pentru a ajuta organismul să distrugă celulele tumorale.
MEPACT se utilizează pentru tratarea osteosarcoamelor (cancer de oase) la copii, adolescenţi şi adulţi tineri. Se utilizează după ce aţi suferit o intervenţie chirurgicală pentru îndepărtarea tumorii şi împreună cu chimioterapia pentru distrugerea celulelor canceroase rămase cu scopul de a reduce riscul revenirii cancerului.
2. ÎNAINTE DE UTILIZAREA MEPACT
Nu folosiţi MEPACT
-dacă sunteţi alergic (hipersensibil) la mifamurtidă sau la oricare dintre celelalte componente ale MEPACT.
-dacă luaţi medicamente care conţin ciclosporină, tacrolimus sau doze mari de AINS (vezi mai jos „Utilizarea altor medicamente”).
Aveţi grijă deosebită când utilizaţi MEPACT
Adresaţi-vă medicului înainte de a utiliza MEPACT, dacă oricare dintre următoarele cazuri este valabil pentru dumneavoastră:
– dacă aveţi sau aţi avut probleme cu inima sau vasele sanguine, precum cheaguri de sânge (tromboze), sângerări (hemoragii) sau inflamarea venelor (vasculită). Va trebui să fiţi supravegheat mai atent pe durata tratamentului cu MEPACT. Dacă aveţi simptome de lungă durată sau care se agravează, adresaţi-vă medicului, deoarece administrarea MEPACT poate necesita amânare sau întrerupere.
– dacă aţi suferit de astm bronşic sau alte tulburări respiratorii. Înainte de a utiliza MEPACT, trebuie să vă adresaţi medicului pentru a vedea dacă trebuie să luaţi tratamentul pentru astm bronşic pe durata utilizării MEPACT.
– dacă aţi suferit de boli inflamatorii sau autoimune sau dacă aţi fost tratat cu corticosteroizi sau alte medicamente care pot influenţa sistemul imunitar.
Utilizarea altor medicamente
Vă rugăm să spuneţi medicului dumneavoastră dacă luaţi sau aţi luat recent orice alte medicamente, inclusiv dintre cele eliberate fără prescripţie medicală. Este deosebit de important ca medicul dumneavoastră să fie informat dacă luaţi medicamente care conţin oricare dintre următoarele substanţe active:
– ciclosporină, tacrolimus, utilizate după un transplant pentru a preveni rejetul organelor transplantate sau alte imunosupresoare utilizate, de exemplu, pentru tratarea psoriazisului (o boală a pielii).
– medicamente antiinflamatoare nesteroidiene (AINS), cum sunt acid acetilsalicilic, ibuprofen sau diclofenac, utilizate pentru tratarea durerilor de cap, febrei sau durerii. Este interzisă administrarea MEPACT împreună cu doze mari de AINS.
– corticosteroizi, utilizaţi pentru tratarea inflamaţiilor, alergiilor sau astmului bronşic. Este interzisă administrarea MEPACT atunci când se folosesc în mod regulat corticosteroizi.
Se recomandă administrarea la momente diferite de MEPACT şi doxorubicină sau alte medicamente dacă sunt administrate în cadrul aceluiaşi regim chimioterapic.
Sarcina şi alăptarea
MEPACT nu a fost studiat la femei gravide. Prin urmare, MEPACT nu trebuie administrat în timpul sarcinii sau la femei care nu folosesc mijloace contraceptive eficace. Trebuie să folosiţi mijloace contraceptive eficace în cazul în care urmaţi un tratament cu MEPACT. Este important să vă informaţi medicul dacă sunteţi gravidă, dacă suspectaţi că sunteţi gravidă sau dacă plănuiţi să rămâneţi gravidă.
Nu se cunoaşte dacă MEPACT este excretat în laptele uman. În cazul în care alăptaţi, trebuie să vă informaţi medicul.
Conducerea vehiculelor şi folosirea utilajelor
Unele dintre reacţiile adverse foarte frecvente sau frecvente ale tratamentului cu MEPACT (cum ar fi ameţeală, vertij, fatigabilitate şi vedere înceţoşată) ar putea influenţa capacitatea de a conduce vehicule sau de a folosi utilaje.
3. CUM SE UTILIZEAZĂ MEPACT
Doze şi schema de administrare
Siguranţa şi eficacitatea MEPACT au fost stabilite la pacienţi cu vârste cuprinse între 2 şi 30 de ani. Doza de MEPACT este de 2 mg mifamurtidă/m2 de suprafaţă corporală. Aceasta vă va fi administrată de două ori pe săptămână (la un interval de cel puţin trei zile) în primele 12 săptămâni, după care vi se va administra o dată pe săptămână timp de încă 24 de săptămâni.
Schema tratamentelor cu MEPACT poate fi ajustată pentru a se potrivi cu schema de chimioterapie. Nu este nevoie să întrerupeţi schema terapeutică cu MEPACT, în cazul în care se amână chimioterapia; trebuie să faceţi 36 de săptămâni (9 luni) de tratament cu MEPACT fără nicio întrerupere.
Cum se administrează MEPACT
Pulberea liofilizată trebuie reconstituită într-o suspensie lichidă, filtrată cu ajutorul filtrului furnizat şi diluată suplimentar înainte de utilizare. MEPACT se administrează apoi sub formă de perfuzie direct în venă (intravenos) pe durata a aproximativ o oră. Această sarcină îi revine medicului sau asistentei, care vă va şi monitoriza în tot acest timp. Administrarea de MEPACT nu necesită spitalizare. Acesta poate fi administrat pacienţilor şi în ambulatoriu.
Dacă utilizaţi mai mult decât trebuie din MEPACT
Puteţi resimţi agravarea reacţiilor adverse, incluzând febră, frisoane, oboseală, greaţă, vărsături, dureri de cap şi hipotensiune sau hipertensiune arterială. În cazul unei supradoze, adresaţi-vă medicului dumneavoastră sau celui mai apropiat spital.
Dacă aveţi orice întrebări suplimentare cu privire la utilizarea acestui produs, adresaţi-vă medicului dumneavoastră.
4. REACŢII ADVERSE POSIBILE
Ca toate medicamentele, MEPACT poate provoca reacţii adverse, cu toate că nu apar la toate persoanele. Majoritatea pacienţilor prezintă frisoane, febră şi fatigabilitate. Acestea sunt de obicei uşoare spre moderate, au un caracter tranzitoriu şi pot fi tratate în mod obişnuit de medicul dumneavoastră, de exemplu folosind paracetamol pentru febră.
Adresaţi-vă imediat medicului:
– dacă aveţi febră sau frisoane care persistă mai mult de 8 ore de la administrarea dozei de MEPACT, deoarece aceasta poate fi un semn de infecţie sau
– dacă aveţi o erupţie cutanată sau orice probleme de respiraţie (stridor).
Reacţiile adverse pot să apară cu anumite frecvenţe, care sunt definite după cum urmează:
- foarte frecvente: afectează mai mult de 1 din 10 utilizatori
- frecvente: afectează 1 până la 10 utilizatori din 100
- mai puţin frecvente: afectează 1 până la 10 utilizatori din 1.000
- rare: afectează 1 până la 10 utilizatori din 10.000
- foarte rare: afectează mai puţin de 1 din 10.000 utilizatori
- cu frecvenţă necunoscută: frecvenţa nu poate fi estimată din datele disponibile.
Reacţii adverse foarte frecvente:
– febră, frisoane/ tremurat, slăbiciune, oboseală sau disconfort general
– greaţă şi/sau vărsături, diaree sau constipaţie
– dureri de cap sau ameţeli
– accelerarea bătăilor inimii
– creşterea sau scăderea tensiunii arteriale
– lipsa poftei de mâncare
– transpiraţie
– dureri, inclusiv dureri generalizate, dureri musculare şi/sau articulare şi dureri de spate, piept, abdomen, braţe sau picioare
– tuse, dificultăţi de respiraţie sau accelerarea respiraţiei
– scăderea temperaturii corpului
– scăderea numărului de globule roşii
Reacţii adverse frecvente:
– colorarea albastră a unor ţesuturi, cum sunt pielea sau gingiile, cauzată de lipsă de oxigen
– creşterea perceptibilă a frecvenţei sau intensităţii bătăilor inimii
– umflarea braţelor sau picioarelor sau orice alte umflături
– disconfort toracic
– indigestie, scăderea apetitului alimentar sau scădere în greutate
– înroşire la locul injectării sau al cateterului, inflamaţie, infecţie sau alte reacţii locale
– erupţie cutanată sau înroşire, inflamaţie a pielii, mâncărime, uscăciunea pielii, paloarea sau înroşirea tranzitorie a pielii
– inflamaţia pielii, tendoanelor, muşchilor sau ţesuturilor similare care susţin structurile organismului
– inflamarea venelor
– dureri în abdomenul superior sau torace, balonare sau dureri abdominale
– alte dureri, inclusiv de ceafă, umăr sau gât
– spasme musculare sau rigiditate musculară
– stare de răceală
– senzaţie de oboseală, ameţeală sau somnolenţă
– arsuri, senzaţie de ciupitură/ mâncărime sau diminuarea sensibilităţii
– mişcări involuntare de tip tremor
– deshidratare
– inflamaţia mucoaselor
– congestia sau inflamaţia nasului, gâtului sau sinusurilor
– infecţii ale tractului respirator superior (cum ar fi guturai) sau ale tractului urinar (cum ar fi infecţiile vezicii urinare)
– infecţii generalizate
– infecţii cu (virusul) Herpes simplex
– tuse productivă, stridor sau dificultăţi de respiraţie exacerbate sau la efort
– expectorare de sânge sau sângerări nazale
– prezenţa de lichide în cavitatea pulmonară
– prezenţa sângelui în urină, dificultăţi sau durere la urinat sau urinat frecvent
– insomnie, depresie, anxietate sau confuzie
– ameţeli
– ţiuit în urechi
– vedere înceţoşată
– căderea părului
– menstruaţii dificile, dureroase
– pierderea auzului
Dacă vreuna dintre reacţiile adverse devine gravă sau dacă observaţi orice reacţie adversă nemenţionată în acest prospect, vă rugăm să-i spuneţi medicului dumneavoastră.
5. CUM SE PĂSTREAZĂ MEPACT
A nu se lăsa la îndemâna şi vederea copiilor. Nu utilizaţi MEPACT după data de expirare înscrisă pe eticheta flaconului şi pe cutie.
Flacoane nedeschise: A se păstra la frigider (2°C – 8°C). A nu se congela. Păstraţi flaconul în cutie pentru a fi protejat de lumină.
Suspensie reconstituită După reconstituire în soluţie de clorură de sodiu 9 mg/ml (0,9%), păstraţi la temperatura camerei (aproximativ între 20ºC – 25ºC) şi utilizaţi în decurs de 6 ore.
6. INFORMAŢII SUPLIMENTARE
Ce conţine MEPACT
– Substanţa activă este mifamurtida. Fiecare flacon conţine 4 mg mifamurtidă. După reconstituire în soluţie perfuzabilă de clorură de sodiu 9 mg (0,9%), fiecare ml de suspensie conţine 0,08 mg mifamurtidă.
– Celelalte componente sunt 1-palmitoil-2-oleoil-sn-glicero-3-fosfocolină (POPC) şi sarea monosodică a 1,2-dioleoil-sn-glicero-3-fosfo-L-serinei (OOPS).
Cum arată MEPACT şi conţinutul ambalajului
MEPACT este o pulbere liofilizată albă până la aproape albă, omogenă pentru suspensie perfuzabilă.
MEPACT este furnizat într-o cutie care conţine:
- Un flacon de 50 ml cu capac opritor gri din cauciuc butilic, cu capsă din aluminiu şi capac protector din plastic.
- Un filtru pentru MEPACT steril, furnizat într-un blister.
Deţinătorul autorizaţiei de punere pe piaţă şi producătorul
Deţinătorul autorizaţiei de punere pe piaţă:
IDM PHARMA SAS 11-15 Quai De Dion Bouton 92816 Puteaux Cedex Franţa
Producător:
Takeda Ireland Ltd Bray Business Park Kilruddery Co. Wicklow Irlanda
Takeda Italia Farmaceutici S.p.A Via Crosa, 86 28065 Cerano (NO) Italia
Informaţii detaliate privind acest medicament sunt disponibile pe website-ul Agenţiei Europene a Medicamentului (EMEA): http://www.emea.europa.eu/.
Acest prospect a fost aprobat în
Următoarele informaţii sunt destinate numai medicilor şi personalului medical:
Instrucţiuni pentru prepararea MEPACT pentru perfuzie intravenoasă
Materiale furnizate în fiecare ambalaj –
- 1 flacon de MEPACT (mifamurtidă)
- 1 filtru pentru MEPACT
Materiale necesare, dar nefurnizate –
- Soluţie injectabilă de clorură de sodiu 9 mg/ml (0,9%), EP/USP, pungă de 100 ml
- O seringă sterilă de unică folosinţă de 60 sau 100 ml cu conector luer lock
- Două ace de injectare sterile cu calibrul mediu de 18
Se recomandă ca reconstituirea suspensiei lipozomale să se efectueze într-o hotă cu flux laminar folosind mănuşi sterile şi tehnici aseptice.
Pulberea liofilizată trebuie lăsată să ajungă la o temperatură între aproximativ 20°C – 25°C înainte de reconstituire, filtrare cu ajutorul filtrului furnizat şi diluare. Aceasta durează de obicei aproximativ 30 minute.
1 Capacul flaconului trebuie îndepărtat, iar opritorul din cauciuc trebuie curăţat folosind un tampon cu alcool.
2 Filtrul trebuie scos din blister, iar capacul trebuie îndepărtat de pe vârful filtrului. Apoi vârful trebuie introdus ferm în septul flaconului, până la fixare. Capacul filtrului cu conector luer nu trebuie îndepărtat în acest moment.
3 Punga de 100 ml soluţie perfuzabilă de clorură de sodiu 9 mg/ml (0,9%), acul şi seringa trebuie despachetate (nu sunt furnizate în ambalaj).
4 Locul în care se va introduce acul în punga cu soluţia perfuzabilă de clorură de sodiu 9 mg/ml (0,9%) trebuie tamponat cu alcool.
5 Folosind acul şi seringa, trebuie extrase din pungă 50 ml de soluţie injectabilă de clorură de sodiu 9 mg/ml (0,9%).
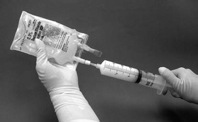
6 După îndepărtarea acului de pe seringă, seringa trebuie ataşată la filtru prin deschiderea capacului filtrului cu conector luer (Figura 1).
1 Soluţia injectabilă de clorură de sodiu 9 mg/ml (0,9%) este adăugată în flacon prin apăsarea lentă, fermă a pistonului seringii. Filtrul şi seringa nu trebuie îndepărtate de pe flacon.
2 Flaconul trebuie să rămână nemişcat timp de un minut pentru a permite hidratarea intensivă a substanţei uscate.
3 Flaconul trebuie apoi agitat ferm timp de un minut, păstrând filtrul şi seringa ataşate. În acest răstimp se formează spontan lipozomii (Figura 2).
10. Doza dorită se poate apoi extrage din flacon prin răsturnarea acestuia şi trăgând încet înapoi de pistonul seringii (Figura 3). Fiecare ml de suspensie reconstituită conţine 0,08 mg mifamurtidă. Volumul de suspensie care trebuie extras pentru dozele necesare se calculează prin următoarea formulă:
Volum de extras = [12,5 x doza calculată (mg)] ml
Pentru uz curent, este furnizat următorul tabel de concordanţă:
11. Seringa trebuie apoi scoasă din filtru, iar un ac nou trebuie montat pe seringa umplută cu suspensie. Locul în care se introduce acul în pungă trebuie tamponat cu alcool, iar suspensia din seringă trebuie injectată în punga iniţială care conţine restul de 50 ml de soluţie injectabilă de clorură de sodiu 9 mg/ml (0,9%) (Figura 4).
- Punga trebuie agitată uşor pentru a amesteca soluţia.
- Datele de identificare ale pacientului, ora şi data trebuie notate pe eticheta pungii care conţine suspensia lipozomală reconstituită, filtratăşi diluată.
- Stabilitatea chimicăşi fizică în timpul utilizării a fost demonstrată pentru 6 ore la temperatura camerei (aproximativ între 20°C – 25°C).
- Din punct de vedere microbiologic, produsul trebuie utilizat imediat. Dacă nu se utilizează imediat, responsabilitatea pentru perioada şi condiţiile de păstrare ale medicamentului în uz îi revine utilizatorului, iar acestea nu trebuie să depăşească, în mod normal, 6 ore la temperatura camerei.
Eliminarea reziduurilor
Fără cerinţe speciale.